Ананасовый ароматизатор напитков имеет формулу
Органическое вещество А имеет запах ананаса и используется в парфюмерии. Оно состоит из трёх элементов и содержит 10,3 % водорода и 27,6 % кислорода по массе. При взаимодействии с водой вещество А превращается в два вещества с неразветвлённым углеродным скелетом, одно из которых — спирт — содержит в 2 раза меньше атомов углерода, чем другое. Определите молекулярную формулу вещества А и установите его структуру. Напишите уравнение щелочного гидролиза А.
1. Определена молекулярная формула вещества А:
2. Вещество А — сложный эфир, причём остаток кислоты в его составе содержит 4 атома углерода (масляная кислота), остаток спирта — 2 атома (этанол). Сложный эфир А — этилбутират:
Кейс "Запахи сложных эфиров" можно использовать как дополнительный материал к урокам химии в 10 классе по теме "Сложные эфиры. Жиры".
Запахи сложных эфиров

Эфиры алифатического ряда имеют в основном фруктовые запахи
Формула сложного эфира Название Аромат
C3H7COOCH2CH2CH(CH3)2 - Изоамилбутират, изоамиловый эфир масляной кислоты – грушевый,
С3Н7СООСН3 – Метилбутанат, метиловый эфир масляной кислоты – яблочный,
С3Н7СООС2Н5 - Этилбутират, Этиловый эфир масляной кислоты и
C3H7COOC4H9 - Бутилбутарат, бутиловый эфир масляной кислоты – ананасовый,
С4Н9СООС2Н5 - Этиловый эфир изовалериановой кислоты – малиновый,
С4Н9СООС5Н11 - Изоамиловый эфир изовалериановой кислоты, изоамилизовалерат - банановый,
С5Н11О(СО)СС3Н7- Бутилпентанат, пентиловый эфир масляной кислоты – абрикос,
HCOOC5H11- Амилформиат, амиловый эфир муравьиной кислоты, – вишня,
CH3COOC8H17 — Октилацетат - запах апельсинов,
Эфиры ароматических кислот имеют бальзамические, животные запахи или запахи экзотических цветов.
Формула сложного эфира Название Аромат
С6Н5СООСН3 –Метилбензоат, метиловый эфир бензойной кислоты – запахи свежего сена, русской кожи (юфти), иланг-иланга, а также туберозы и гвоздики. Имеет резкий, цветочный запах,
С6Н5СООС5Н11 - Пентилбензоат (амилбензоат, бензойноамиловый эфир) - пахнет клевером и амброй – своеобразным выделением из пищеварительного тракта кита,
HCOOCH2CH2C6H5 — 2-фенилэтилформиат - запах хризантем,
ЦИТРОНЕЛЛИЛАЦЕТАТ – компонент эфирного масла герани.
I. Состав и строение сложных эфиров
Сложные эфиры – функциональные производные карбоновых кислот, в молекулах которых гидроксильная группа (-ОН) замещена на остаток спирта (-OR).
Сложные эфиры карбоновых кислот – соединения с общей формулой R–COOR', где R и R' – углеводородные радикалы.

II. Физические свойства и нахождение сложных эфиров в природе
- Летучие, бесцветные жидкости
- Плохо растворимы в воде
- Чаще с приятным запахом
- Легче воды

Сложные эфиры содержатся в цветах, фруктах, ягодах.
Они определяют их специфический запах.
Являются составной частью эфирных масел (известно около 3000 эф.м. – апельсиновое, лавандовое, розовое и т. д.)
Эфиры низших карбоновых кислот и низших одноатомных спиртов имеют приятный запах цветов, ягод и фруктов. Эфиры высших одноосновных кислот и высших одноатомных спиртов – основа природных восков. Например, пчелиный воск содержит сложный эфир пальмитиновой кислоты и мирицилового спирта (мирицилпальмитат):
Аромат.
Структурная формула.
Название сложного эфира
Яблоко

Вишня

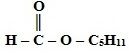
Амиловый эфир муравьиной кислоты
Груша

Изоамиловый эфир уксусной кислоты
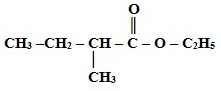
Ананас

Этиловый эфир масляной кислоты
Банан

Изобутиловый эфир уксусной кислоты
(у изоамилацетата так же напоминает запах банана)
Жасмин


Бензиловый эфир уксусной (бензилацетат)
Запахи эфиров:


Сложные эфиры нерастворимы в воде, но хорошо смешиваются со многими органическими веществами. Именно поэтому они используются как растворители для лаков и красок. Рис. 1. Этилацетат и метил ацетат – основа растворителя – жидкости для снятия лака с ногтей.
Температуры кипения сложных эфиров меньше, чем температуры кипения кислот и спиртов с близкой молярной массой. Почему? Сложные эфиры, в отличие от кислот и спиртов, не способны образовывать водородные связи между молекулами.

Сравнение температуры кипения эфиров
III. Номенклатура сложных эфиров
Краткие названия сложных эфиров строятся по названию радикала (R') в остатке спирта и названию группы RCOO - в остатке кислоты. Например, этиловый эфир уксусной кислоты CH3COOC2H5 называется этилацетат.
Названия по ИЮПАК выделены жирным шрифтом:
Этилформиат, этилметаноат;
этиловый эфир муравьиной кислоты
Метилацетат, метилэтаноат;
метиловый эфир уксусной кислоты
Этилбутират, этилбутаноат;
этиловый эфир бутановой кислоты

IV. Применение
- В качестве отдушек и усилителей запаха в пищевой и парфюмерной (изготовление мыла, духов, кремов) промышленности;
- В производстве пластмасс, резины в качестве пластификаторов.
Пластификаторы – вещества, которые вводят в состав полимерных материалов для придания (или повышения) эластичности и (или) пластичности при переработке и эксплуатации.

Применение в медицине
В конце XIX — начале ХХ века, когда органический синтез делал свои первые шаги, было синтезировано и испытано фармакологами множество сложных эфиров. Они стали основой таких лекарственных средств, как салол, валидол и др. Как местнораздражающее и обезболивающее средство широко использовался метилсалицилат, в настоящее время практически вытесненный более эффективными средствами.
V. Получение сложных эфиров
Cложные эфиры могут быть получены при взаимодействии карбоновых кислот со спиртами (реакция этерификации). Катализаторами являются минеральные кислоты.
Реакция этерификации в условиях кислотного катализа обратима. Обратный процесс – расщепление сложного эфира при действии воды с образованием карбоновой кислоты и спирта – называют гидролизом сложного эфира.
Гидролиз в присутствии щелочи протекает необратимо (т.к. образующийся отрицательно заряженный карбоксилат-анион RCOO – не вступает в реакцию с нуклеофильным реагентом – спиртом).
Эта реакция называется омылением сложных эфиров (по аналогии со щелочным гидролизом сложноэфирных связей в жирах при получении мыла).

Материалы для проверки знаний.
Скачать:
| Вложение | Размер |
|---|---|
| slozhnye_efiry._zhiry.ppt | 175.5 КБ |
Подписи к слайдам:
Сложные эфиры. Жиры. Краснодарский край Абинский район учитель высшей категории МОУ СОШ №1 СЕРГЕЕВА ИРИНА АЛЕКСЕЕВНА Поурочные тесты, подготовка к ЕГЭ СН 3 -СН 2 -СОО-СН 3 СН 2 -О-СО-С 17 Н 33 СН-О-СО-С 17 Н 33 СН 2 -О-СО-С 17 Н 33 О С О =
1. Как назвывается реакция между карбоновой кислотой и спиртом? 2. C оотнесите: исходные вещества: 1) метановая кислота и муравьиный спирт, 2) ацетат серебра и 2- бромпропан, 3) масляная кислота и 2- метилпропанол-1, 4) хлорангидрид пропионовой кислоты и фенол; ответ: продукт реакции: А) фениловый эфир уксусной кислоты, Б) метиловый эфир муравьиной кислоты , В) изопропиловый эфир уксусной кислоты, Г) изобутиловый эфир масляной кислоты. Напишите уравнения реакций. Какая из них является обра-тимой? Назовите продукты реакции по международной номенкла-туре.
3. В состав природных жиров не входит кислота: 1) щавелевая 2) стеариновая 3) масляная 4) олеиновая 4. Что такое воск ? Соединение какой структуры можно отнести к воскам? 1) СН 3 СООС 16 Н 33 2) С 15 Н 31 СООС 16 Н 33 3) С 15 Н 31 СООС 2 Н 5 4) СН 2 = СН-СООС 3 Н 7 5. Химическое равновесие в системе СН 3 -СООН (ж) + С 2 Н 5 ОН (ж) СН 3 -СООС 2 Н 5 (ж) + Н 2 О (ж) + Q можно сместить вправо : 1) удалением воды 2) введением катализатора 3) увеличением давления 4) увеличением температуры .
6. Сложные эфиры плохо растворимы в воде и обладают меньшими температурами кипения по сравнению с изомер-ными им кислотами. Причина этого: 1) меньшая длина углеводородного радикала, связанного с карбоксильным атомом углерода; 2) отсутствие межмолекулярных водородных связей; 3) наличие атома углерода в sp 2- гибридном состоянии; 4) верного ответа среди перечисленных нет. 7. Ананасовый ароматизатор напитков имеет формулу СН 3 -СН 2 -СН 2 -СООС 2 Н 5 . Название этого сложного эфира: 1) этилформиат 2) этилбутират 3) этилпропионат 4) верного ответа нет 2 2
8. В основе процесса переработки жидких растительных масел в твердые жиры лежит реакция: 1) гидрирования 2) гидратации 3) гидролиза 4) омыления 9. Органическое стекло получают полимеризацией метилового эфира 2- метилпропеновой кислоты. Элементарное звено полимера имеет относительную молекулярную массу: 1) 72 2) 86 3) 100 4) 102 10. Растительное масло ( условно чистый триолеат глицерина) массой 1 т подвергли каталитическому гидрированию и получили саломас с выходом 90 %. Сколько пачек маргарина по 250 г можно изготовить из этого количества саломаса, если его содержание в маргарине 80 %? 1) 4530 2) 4020 3) 3620 4) 3260
11. Гидролизом жиров можно получить: 1) высшие спирты 2) этиленгликоль 3) непредельные альдегиды 4) глицерин 12. Какую массу глицерина можно получить из природного жира массой 17,75 кг, содержащего 97% тристеарата глицерина? 1) 1,78 кг 2) 1,84 кг 3) 1,90 кг 4) 2,26 кг 13. Какая масса муравьиной кислоты и этилового спирта потребуется для получения 296 г сложного эфира, если выход этого продукта реакции составляет 80% от теоретического? 1) по 184 г 2) по 230 г 3) по 288 г 4) 300 г кислоты, 230 г спирта
14. Соотнесите: группа веществ: 1) воски 2) жиры 3) мыла 4) сложные эфиры природа вещества: А) сложные эфиры глицерина и высших карбоновых кислот, Б) сложные эфиры высших карбоновых кислот и высших спиртов, Г) натриевые и калиевые соли высших карбоновых кислот, Д) производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал.
15. Исключите лишнее вещество: 1) стеарат натрия 2) трипальмитат глицерина 3) триолеат глицерина 4) тристеарат глицерина 16. Сколько граммов этилового эфира уксусной кислоты можно получить из 11,5 г этанола и 30 г уксусной кислоты, если выход реакции составляет 80 % от теоретического? 1) 17, 6 г 2) 27,5 г 3) 35,2 г 4 ) 55,0 г 17. Какую массу триолеата глицерина необходимо подвергнуть гидролизу для получения 42,3 г олеиновой кислоты? 1) 14,7 г 2) 22,1 г 3) 44,2 г 4) 132,6 г
2. C оотнесите: исходные вещества: 1) метановая кислота и муравьиный спирт, 2) ацетат серебра и 2- бромпропан, 3) масляная кислота и 2- метилпропанол-1, 4) хлорангидрид пропионовой кислоты и фенол; продукт реакции: А) фениловый эфир уксусной кислоты, Б) метиловый эфир муравьиной кислоты , В) изопропиловый эфир уксусной кислоты, Г) изобутиловый эфир масляной кислоты. Напишите уравнения реакций. Какая из них является обратимой?
Воски- сложные эфиры высших карбоновых кислот и высших спиртов.
Саломас - продукт гидрогени - зации жидких жиров.
Маргарин- пищевой жир. Состоит из смеси гидрогени - зированных масел, животных жиров, молока и некоторых других веществ ( соли, саха - ра, витаминов и др).
Н-СООН + НО-С2Н5 Н-СОО-С2Н5 + Н2О m теор = 296 : 0,8= 340 г х= =230 г 370 г х г х г 1 моль 46 г/моль 46 г 1 моль 46 г/моль 46 г 1 моль 74 г/моль 74 г 46 г * 370 г 74 г
Презентация была опубликована 6 лет назад пользователемДанила Щапов
Презентация на тему: " Санкт-Петербург Боголюбова И.В.. Н 2 О + О R 1 – С R 1 – С О – R 2 О – R 2 сложный эфир О R 1 – С + R 1 – С + О–Н О–Н Н Н спирт – О–R 2 – О–R 2 О–R 2." — Транскрипт:
1 Санкт-Петербург Боголюбова И.В.
3 Н 2 О + О R 1 – С R 1 – С О – R 2 О – R 2 сложный эфир О Н – С О – С 2 Н 5 О – С 2 Н 5 этиловый эфир (запах рома) О С 3 Н 7 – С О – СН 3 О – СН 3 метиловый эфир (запах яблок) муравьиной кислоты масляной кислоты О R 1 – С + R 1 – С + О–Н О–Н Н спирт – О–R 2 – О–R 2 Схема образования сл.эфиров к.к-та Номенклатура
4 О R 1 – С R 1 – С О – R 2 О – R 2 сложный эфир + Н-ОН НО Н О R 1 – С R 1 – С О–Н О–Нк.к-та + Н – О–R 2 спирт Гидролиз сл.эфиров
5 л лл л ц цц ц р рр р Г ГГ Г и ии и е ее е и ии и н нн н Жирная кислота Жир
6 Функции жиров: 2) источник энергии (энергетическая ценность жиров в 2 раза выше, чем у углеводов); 3) Термоизолятор для китов и тюленей; 1) структурная функция;
7 Марселен Пьер Эжен Бертло ( ) ( ) французский физикохимик французский физикохимик Мишель Эжен Шеврель ( ) ( ) французский химик французский химик СССглицерин Жирные кислоты Предельные ПредельныеНепредельные С 15 Н 31 СООН пальмитиновая кислота С 17 Н 35 СООН стеариновая кислота С 17 Н 33 СООН олеиновая кислота С 17 Н 31 СООН линолевая кислота С 17 Н 29 СООН линоленовая кислота С – ОН СН 2 – ОН СН – ОН СН 2 – ОН С – ОН Составляюшие жира СН 2 – ОН С – ОН СН 2 – ОН С – ОН СН 2 – ОН СН – ОН С – ОН СН 2 – ОН СН – ОН С – ОН
8 ССС ССС С – О– Н Н Н Н Н Н О –С – R 1 НО НО О –С – R 2 –С – R 2НО О –С – R 3 НО + + О –С –С 15 Н 31 НО О –С –С 17 Н 31 НО О –С –С 17 Н 29 ф-т ф-т Н НО Н НО ННО С – О– СН 2 – О– С – О– СН 2 – О– С – О– СН 2 – О– СН – О– С – О– СН 2 – О– СН – О– С – О– СН 2 – О– СН – О– СН 2 – О– С – О– СН 2 – О– СН – О– С – О– СН 2 – О– СН – О– СН 2 – О– ННО Н НО Н НО 3Н 2 О + СН 2 –О– СН –О– СН 2 –О– О С – R 1 С – R 1 О С – R 2 С – R 2 О С – R 3 С – R 3 СН 2 –О– СН –О– СН 2 –О– О С – R 1 С – R 1 О С – R 2 С – R 2 жир СН 2 –О– СН –О– СН 2 –О– О С – С 15 Н 31 С – С 15 Н 31 О С –С 17 Н 31 С –С 17 Н 31 О С –С 17 Н 29 С –С 17 Н 29 Н Н Н О С – R 3 С – R 3 НО – О С – R 1 С – R 1 НО – О С – R 2 С – R 2 + НО– Н Н Н О –С –С 15 Н 31 НО О –С –С 17 Н 31 + НО О –С –С 17 Н 29 –С –С 17 Н 29НО глицерин ж.к-ты Схема образ-ия жира
9 К–О–Н К–О–Н + К–О–Н К–О–Н К–О–Н СН 2 –О– СН –О– СН 2 –О– О С – R С – R О О О 3R-С–О-К 3R-С–О-К СН 2 –О–Н СН 2 –О–Н + СН –О–Н + СН –О–Н СН 2 –О–Н СН 2 –О–Нмыло СН 2 –О– СН –О– СН 2 –О– О С – R С – R О О Н–О–Н Н–О–Н + Н–О–Н Н–О–Н Н–О–Н О 3R-С-ОН + СН 2 –О–Н СН –О–Н СН 2 –О–Н ф-т t˚ ИЛИ Ф – Т жир глицерин ж.к-ты Гидролиз жиров Омыление жиров Н ОН Н ОК или t o
10 СН 2 –О – СН –О – СН 2 –О – О С – С 15 Н 31 С – С 15 Н 31 О С –С 17 Н 31 С –С 17 Н 31 О С –С 17 Н 29 С –С 17 Н 29 + Н 2 5 t˚К СН 2 –О – СН –О – СН 2 –О – Гидрирование жиров Гидрирование жиров СН 2 –О – СН –О – СН 2 –О – О С – С – О О С 15 Н 31 С 15 Н 31 С 17 Н 35 С 17 Н 35 жидкий жир (растительный) твердый жир (аналог животного жира)
11 К + + О R – С – О ̅ R – С – О ̅ О R – С – О-К R – С – О-К R СОО ̅ гидрофобный гидрофобный гидрофильный гидрофильный грязь вода Н2ОН2ОН2ОН2О грязь грязь R СОО ̅ грязь О R – С – О ̅ R – С – О ̅ Моющее действие мыла
12 R–СН 2 – О–Н + –О–SО 2 –О–Н –О–SО 2 –О–НН высший спирт серная кислота О–Н + Н Н 2 О + R–СН 2 – О–SО 2 –О–Н кислый сернокислый эфир –О–SО 2 –О–Н –О–SО 2 –О–Н R–СН 2 – О–Н + Н R–СН 2 – О–SО 2 –О– Na – Н OH Н + OH Н 2 О + Na R–СН 2 – О–SО 2 –О– СМС Н + OH Схема образования СМС – Na Na –
13 Укажите формулу сложного эфира О а) Н-С О-С 3 Н 7 О б) С 3 Н 7 - С С 3 Н 7 в) СН 3 – О – С 2 Н 5 О г) С 2 Н 5 - С ОН
14 Какая формула соответствует пропиловому эфиру масляной кислоты? О О а) С 3 Н 7 - С б) СН 3 - С О-С 2 Н 5 О-С 3 Н 7 О в) Н-С О-С 2 Н 5 О г) С 3 Н 7 - С О-С 3 Н 7
15 Ананасовый ароматизатор напитков имеет формулу: СН 3 – СН 2 – СН 2 – СООС 2 Н 5 а) этилформиат; б) этилбутират; в) этилпропионат; г) верного ответа среди перечисленных нет.
16 Соотнесите: 1)растит.жир 2)животн.жир 3)жидкое мыло 4)тверд. мыло 5)СМС формулы: а) С 17 Н 35 СООNa б) С 17 Н 29 СООК в) С 12 Н 25 ОSО 2 ONa г)СН 2 -О-СО-С 17 Н 31 д)СН 2 -О-СО-С 17 Н 35 СН-О-СО-С 17 Н 29 СН-О-СО-С 15 Н 31 СН 2 -О-СО-С 17 Н 29 СН 2 -О-СО-С 15 Н 31
17 3) С 3 Н 7 -СООСН 3 + Н 2 О 1) СН 2 -О-СО-С 17 Н 31 СН-О-СО-С 17 Н 29 + n H 2 СН 2 -О-СО-С 17 Н 29 2) СН 2 -О-СО-С 17 Н 35 СН-О-СО-С 15 Н КОН СН 2 -О-СО-С 15 Н 31 4) С 4 Н 9 СООН + С 2 Н 5 ОН Соотнесите: исходные вещества типы реакций: а) омыление в) этерификация б) гидрирование г) гидролиз
18 Средство для отпугивания комаров (репеллент) синтезируют по схеме: сн 3 сн 3 окисл. 2сн 3 он 1 2 формулы веществ 1 и 2: а)соосн 3 б)соон в)соон г)осн 3 соосн 3 соон соосн 3 осн 3
19 Главное моющее действие мыла: 1) щелочное действие; 2) растворение грязи; 3) повышение смачиваемости загрязнения водой.
20 Соотнесите недостатки: 1)мыла; 2)СМС: а) нельзя использовать в жесткой воде; б) образующаяся при гидролизе щелочь портит объект стирки; в) портит экологию; г) использование пищевого сырья;
21 Составьте жир из глицерина и следующих кислот и прогидрируйте его Олеиновая к-та Линоленовая к-та Пальмитиновая к-та 1) Стеариновая к-та Линолевая к-та 2) Олеиновая к-та Линолевая к-та Пальмитиновая к-та 3) 4) Олеиновая к-та Линолевая к-та Линоленовая к-та 5) Стеариновая к-та Линолевая к-та Пальмитиновая к-та 6) Олеиновая к-та Линоленовая к-та 7) Пальмитиновая к-та Олеиновая к-та 8) Линоленовая к-та Олеиновая к-та Стеариновая к-та

Номенклатура
- CH3COOH – метилформиат;
- HCOOCH3 – этилформиат;
- CH3COOC4H9 – бутилацетат;
- CH3-CH2-COO-C4H9 – бутилпропионат;
- CH3-SO4-CH3 – диметилсульфат.
Также используются тривиальные названия кислоты, входящей в состав соединения:
- С3Н7СООС5Н11 – амиловый эфир масляной кислоты;
- HCOOCH3 – метиловый эфир муравьиной кислоты;
- CH3-COO-CH2-CH(CH3)2 – изобутиловый эфир уксусной кислоты.

Рис. 1. Структурные формулы сложных эфиров с названиями.
Классификация
В зависимости от происхождения сложные эфиры делятся на две группы:
- эфиры карбоновых кислот – содержат углеводородные радикалы;
- эфиры неорганических кислот – включают остаток минеральных солей (C2H5OSO2OH, (CH3O)P(O)(OH)2, C2H5ONO).
Наиболее разнообразны сложные эфиры карбоновых кислот. От сложности строения зависят их физические свойства. Эфиры низших карбоновых кислот – летучие жидкости с приятным ароматом, высших – твёрдые вещества. Это плохо растворимые соединения, плавающие на поверхности воды.
Виды сложных эфиров карбоновых кислот приведены в таблице.
Описание
Примеры
Жидкости, молекулы которых включают не более восьми атомов углерода. Обладают фруктовым ароматом. Состоят из одноатомных спиртов и карбоновых кислот
Жидкие (масла) и твёрдые вещества, содержащие от девяти до 19 атомов углерода. Состоят из глицерина и остатков карбоновых (жирных) кислот
Оливковое масло – смесь глицерина с остатками пальмитиновой, стеариновой, олеиновой, линолевой кислот
Твёрдые вещества с 15-45 атомами углерода

Сложные эфиры карбоновых кислот – главная составляющая ароматных эфирных масел, которые содержатся в плодах, цветах, ягодах. Также входят в состав пчелиного воска.

Рис. 3. Эфирные масла.
Получение
Получают сложные эфиры несколькими способами:
-
реакцией этерификации карбоновых кислот со спиртами:
Свойства
Химические свойства сложных эфиров обусловлены функциональной группой -COOH. Основные свойства сложных эфиров описаны в таблице.
Реакция
Описание
Уравнение
При нагревании в воде разлагаются на кислоту и спирт. Под действием раствора щёлочи образуются соль и спирт
Реакция возможна при наличии кратных связей
Радикалы замещаются остатками спиртов и аминогруппой
Сложные эфиры используются в косметологии, медицине, пищевой промышленности в качестве ароматизаторов, растворителей, наполнителей.
Что мы узнали?
Из темы урока химии 10 класса узнали, что такое сложные эфиры. Это соединения, включающие два радикала и карбоксильную группу. В зависимости от происхождения могут содержать остатки минеральных или карбоновых кислот. Сложные эфиры карбоновых кислот делятся на три группы: жиры, воски, фруктовые эфиры. Это плохо растворимые в воде вещества с небольшой плотностью и приятным ароматом. Сложные эфиры реагируют со щелочами, водой, галогенами, спиртами и аммиаком.
Тест по теме
Средняя оценка: 4.6 . Всего получено оценок: 249.
Не понравилось? - Напиши в комментариях, чего не хватает.
Содержание
- Номенклатура
- Классификация
- Получение
- Свойства
- Что мы узнали?
- Тест по теме
- Предельные одноатомные спирты
- Одноатомные спирты
- Спирты. Фенолы
- Альдегиды и кетоны
- Получение альдегидов
- Глюкоза
- Сахароза
- Альдегиды
- Триглицериды
- Алкадиены
- Нуклеиновые кислоты
- Циклоалканы
- Изомерия Сложные эфиры
- Многоатомные спирты
- Химические свойства альдегидов
- Окисление альдегидов
- Уксусный альдегид
- Гидролиз сахарозы
- Органические кислоты
- Свойства сложных эфиров (химические)
- Аминокислоты
- Углеводы
- Целлюлоза
- Крахмал
- Фенол

По многочисленным просьбам теперь можно: сохранять все свои результаты, получать баллы и участвовать в общем рейтинге.
- 1.
![]()
Катя Деева 677 - 2.
![]()
Likazi Likazi 623 - 3.
![]()
Егор Семененко 281 - 4.
![]()
Lilnait Student 203 - 5.
![]()
Марина Захаренко 137 - 6.
![]()
Илья Лисичкин 93 - 7.
![]()
Максим Куликов 93 - 8.
![]()
Тимофей Горшенев 90 - 9.
![]()
Светлана Байтрак 89 - 10.
![]()
Елена Васильева 88
- 1.
![]()
Кристина Волосочева 19,120 - 2.
![]()
Ekaterina 18,721 - 3.
![]()
Юлия Бронникова 18,580 - 4.
![]()
Darth Vader 17,856 - 5.
![]()
Алина Сайбель 16,787 - 6.
![]()
Мария Николаевна 15,775 - 7.
![]()
Лариса Самодурова 15,735 - 8.
![]()
Liza 15,165 - 9.
![]()
TorkMen 14,876 - 10.
![]()
Влад Лубенков 13,530
Самые активные участники недели:
- 1. Виктория Нойманн - подарочная карта книжного магазина на 500 рублей.
- 2. Bulat Sadykov - подарочная карта книжного магазина на 500 рублей.
- 3. Дарья Волкова - подарочная карта книжного магазина на 500 рублей.
Три счастливчика, которые прошли хотя бы 1 тест:
- 1. Наталья Старостина - подарочная карта книжного магазина на 500 рублей.
- 2. Николай З - подарочная карта книжного магазина на 500 рублей.
- 3. Давид Мельников - подарочная карта книжного магазина на 500 рублей.
Карты электронные(код), они будут отправлены в ближайшие дни сообщением Вконтакте или электронным письмом.
Читайте также:

